POSITION PAPER
2022
HTA E PROGRAMMI DI SCREENING NEONATALE
CONTESTO
L’Health Technology Assessment (HTA), come recentemente affermato anche a livello di Unione Europea, è un processo scientifico multidisciplinare basato sull’evidenza che consente alle autorità competenti di determinare l’efficacia relativa delle tecnologie sanitarie nuove o esistenti. L’HTA si concentra specificamente sul Valore aggiunto di una tecnologia sanitaria rispetto ad altre tecnologie sanitarie nuove o esistenti, in termini di efficacia/sicurezza, ma anche di sostenibilità economico-organizzativa e di compatibilità con i valori sociali e l’assetto giuridico del territorio in cui l’HTA è svolto. L’HTA è in grado di contribuire alla promozione dell’innovazione, che offre i migliori risultati per i pazienti e per la società nel suo insieme, ed è uno strumento importante per garantire l’appropriata applicazione ed utilizzo delle tecnologie sanitarie.
Sono innumerevoli, in Italia, le evidenze e gli studi che dimostrano in maniera netta come proprio grazie alle valutazioni di HTA il sistema sanitario è riuscito a garantire con una certa celerità l’introduzione di tecnologie innovative e l’accesso alle stesse da parte dei pazienti così da permettere un miglioramento del livello di salute dei cittadini accompagnato da una sostenibilità del sistema dal punto di vista economico e finanziario.
In particolare, l’affermazione ed implementazione sempre crescente dei programmi di prevenzione e di screening oncologico (per i tumori del colon retto, mammella e cervice uterina), che ha permesso, e continua a permettere, di ottenere risultati molto importanti in termini di sanità pubblica e a tutela della salute dei cittadini, è stata possibile proprio grazie allo sviluppo delle valutazioni HTA, che hanno fornito ai decisori gli elementi per determinare il reale Valore aggiunto di questi interventi e delle tecnologie utilizzate, così da poter individuare le risorse da investire. Infatti, proprio grazie ai programmi di screening validati si è stati in grado di diagnosticare precocemente determinate malattie, poter trattare tempestivamente i pazienti con conseguente riduzione della disabilità e delle conseguenze nefaste di queste patologie. Il tutto garantendo una elevata qualità e appropriatezza, un favorevole rapporto beneficio rischio e una capacità di introdurre tempestivamente le innovazioni promettenti, come nel caso del test HPV per lo screening della cervice uterina e della conseguente valutazione dell’efficienza, adottato in Italia, in anticipo rispetto ad altri paesi europei, sulla base di una rigorosa valutazione HTA. –1,2-
PROBLEMATICA
Nonostante queste evidenze, ancora persiste purtroppo un ritardo, in alcuni ambiti decisionali, nel ritenere l’HTA lo strumento più adeguato per investire le risorse a disposizione e garantire un accesso rapido alle tecnologie.
Quanto contenuto nella Legge di stabilità in relazione allo Screening Neonatale Esteso (SNE) ne è l’esempio paradigmatico. La decisione, infatti, di emendare quanto previsto dal comma 2, articolo 4, della legge 19 agosto 2016, n. 167 (l’Age.na.s. compie una valutazione di HTA su quali tipi di screening neonatale effettuare) stupisce la comunità scientifica, e la Sihta nello specifico, proprio alla luce del fatto che la valutazione di HTA, come avviene solitamente, avrebbe permesso di rendere disponibili le evidenze relative alle tipologie di screening da effettuare anche con riferimento alle risorse necessarie per rendere questa prestazione efficiente oltreché efficace. In assenza di una valutazione di HTA si navigherà a vista con il rischio di non riuscire ad individuare il miglior percorso tanto nell’interesse dei pazienti che del sistema sanitario in termini di sostenibilità.
L’eliminazione della obbligatorietà di effettuare valutazioni HTA per l’introduzione di nuovi test nel pannello per lo SNE a parere della nostra Società Scientifica è, quindi, un emendato controcorrente, sia rispetto a tutto quello che invece è il quadro normativo europeo (HTA Regulation approvato dal Parlamento Europeo il 13/12/2021–3-), che a quanto previsto dalla Legge 53/2021–4- all’articolo 15 e dalla Legge 208/2015–5- al comma 557 per quanto riguarda l’aggiornamento dei Livelli Essenziali di Assistenza.
In sostanza, la proposta di emendamento, oltre ad essere controcorrente con quanto previsto dalla Legge 208, non andrebbe altro che a ritardare l’inserimento dei nuovi test nel programma SNE.
Infatti, poi, almeno a norma di legge, la Commissione LEA “…si avvale delle valutazioni HTA su tecnologie sanitarie e biomediche e su modelli e procedure organizzativi…”, “…valuta l’impatto economico delle modifiche LEA”, e “valuta che l’applicazione dei LEA avvenga in tutte le regioni con lo stesso standard di qualità..:”.
In un contesto complesso ed articolato come quello degli screening neonatali, in cui l’utilizzo delle tecnologie diagnostiche è fortemente connesso con i modelli organizzativi dello screening, l’assenza di una valutazione multidimensionale come quella HTA, che lega l’efficacia ai costi, all’organizzazione oltre che agli impatti etici, sociali e giuridici, genera il rischio di introdurre gli screening in una maniera disomogenea e disarticolata nei diversi contesti regionali, riducendone la potenziale efficacia e creando differenze nella equità di accesso nelle diverse realtà territoriali, oltre che potenziali rischi di prestazioni inappropriate.
Per evitare questo la Commissione nazionale per l’aggiornamento dei LEA, ai sensi appunto del comma 557 della legge 208 dovrebbe poi comunque procedere ad una valutazione HTA che, non essendo fatta prima (a seguito di quanto emendato), andrebbe fatta dopo quando la proposta arriva in sede di Comitato LEA dilazionando così ulteriormente i tempi, con evidenti ricadute negative per i pazienti e la società nel suo complesso.
FOCUS
Come Società Scientifica non possiamo far notare come forse sia arrivato il momento nel nostro Paese di fare chiarezza su come si intendano prendere importanti decisioni di politica sanitaria e di allocazione delle risorse: se dare peso all’evidenza scientifica – ascoltando il parere degli stakeholder in un processo regolato e tempestivo – oppure lasciare spazio a decisioni basate sulla convenienza politica di questa o quella parte o di alcuni portatori di interesse in quel momento più forti di altri che, però, non necessariamente assicurerebbero il bene comune. Non si può continuare, a nostro avviso, a dare indicazioni contraddittorie sul ruolo che l’HTA deve avere nel contesto del nostro SSN.
Noi siamo convinti che l’avvio e l’implementazione di un sistema di HTA che sia realmente in grado di svolgere il proprio compito non è più procrastinabile. È arrivato il momento di dire con chiarezza se vi è o meno l’intenzione di avviare una attività di HTA come già fanno la maggior parte di tutti i Paesi con sistemi sanitari di tipo universalistico come il nostro e maggiormente sviluppati. Ed è importante far comprendere ai cittadini che fare HTA non vuol dire frenare l’innovazione, ma è lo strumento per accelerare l’adozione di ciò che è realmente di valore.
E se questa intenzione vi è, allora debbono essere implementate tutte quelle azioni previste dalle norme come, ad esempio, quello di avviare in maniera operativa il Programma Nazionale HTA, come previsto dalla Legge 53/2021 con risorse adeguate come previsto dalla stessa legge e per cui è necessario che sia emanato un decreto delegato di cui siamo in attesa dallo scorso aprile 2021, oppure di implementare l’Agenzia Italiana di HTA che SIHTA ha proposto nel 2020 a seguito delle decisioni prese in sede di Conferenza Stato-Regioni con l’ultimo Patto per la Salute del 2019.
Consiglio Direttivo SIHTA
NOTE
1. Ronco G et al. HTA report. Ricerca del DNA del Papilloma Virus umano come test primario per lo screening dei precursori del cancro del collo dell’utero Epidemiologia e Prevenzione 2012; 36 (3-4. S1)
2. Mennini FS, et al. Governance of preventive Health Intervention and On time Verification of its Efficiency: the GIOVE Study. BMJ Open, 2012, DOI: 10.1136/bmjopen-2011-000736
3. Regolamento (UE) 2021/2282 del Parlamento europeo e del Consiglio del 15 dicembre 2021 relativo alla valutazione delle tecnologie sanitarie e che modifica la direttiva 2011/24/UE. Gazzetta Ufficiale della Unione Europea del 22/12/2021. In: https://eur-lex.europa.eu/legal-content/IT/TXT/?uri=OJ:L:2021:458:TOC
4. LEGGE 22 aprile 2021, n. 53. Delega al Governo per il recepimento delle direttive europee e l’attuazione di altri atti dell’Unione europea – Legge di delegazione europea 2019-2020. (21G00063) (GU Serie Generale n.97 del 23-04-2021). In: https://www.gazzettaufficiale.it/eli/id/2021/04/23/21G00063/SG
5. LEGGE 28 dicembre 2015, n. 208.Disposizioni per la formazione del bilancio annuale e pluriennale dello Stato (legge di stabilità 2016). (15G00222) (GU Serie Generale n.302 del 30-12-2015 – Suppl. Ordinario n. 70). In: https://www.gazzettaufficiale.it/eli/id/2015/12/30/15G00222/sg
2020
PER UN SISTEMA ITALIANO DI HEALTH TECHNOLOGY ASSESSMENT (HTA)
PREMESSA
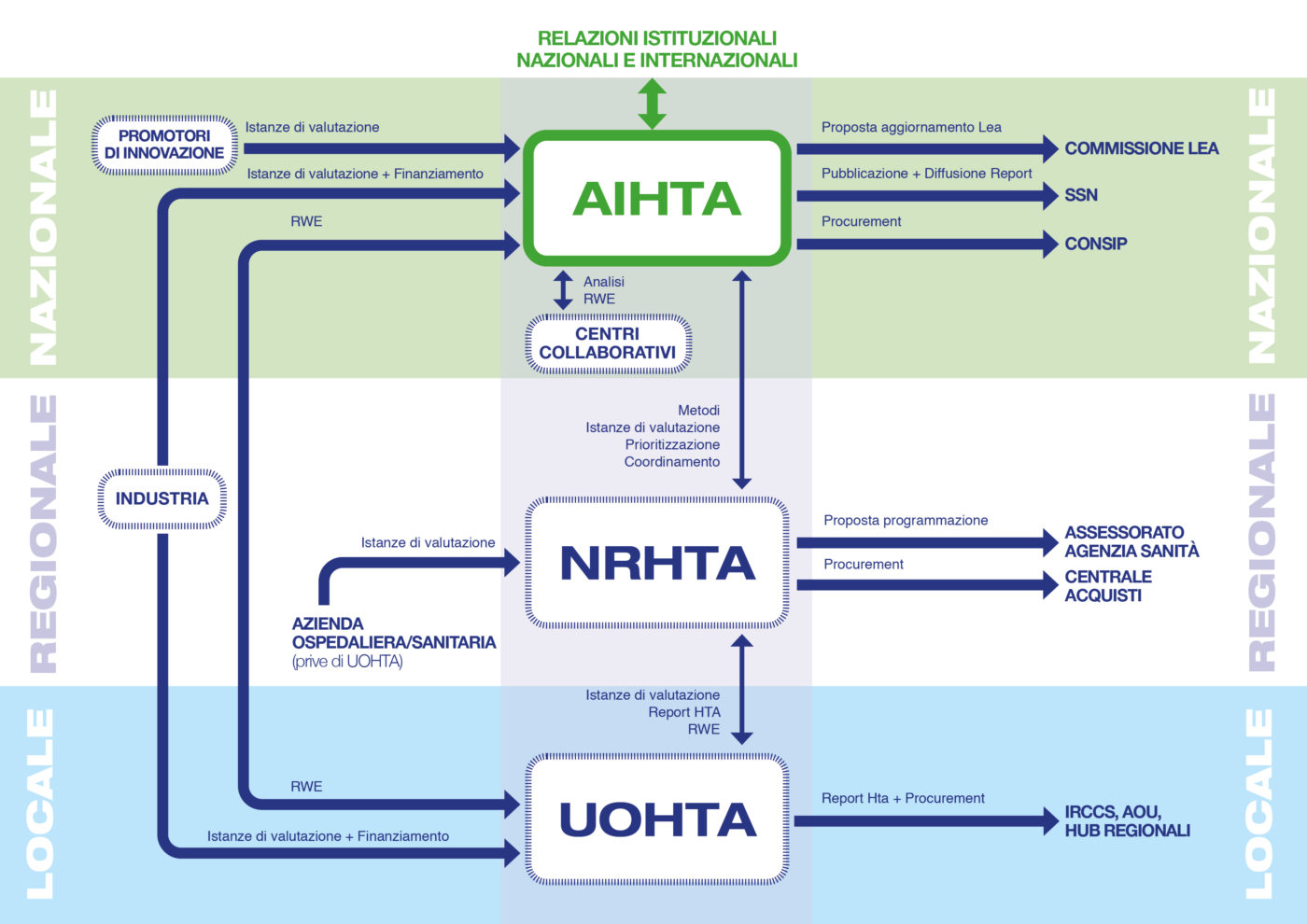
Il documento si pone l’obiettivo di indicare una traiettoria di evoluzione delle attività di HTA in Italia, evoluzione che, a partire dalle esistenti ma frammentate esperienze nazionali e regionali, e nel confronto con le migliori esperienze internazionali, porti alla definizione di un “sistema italiano di HTA” strategicamente concepito per il governo delle tecnologie sanitarie a beneficio del Servizio Sanitario Nazionale (SSN).
La proposta, delineata nei suoi concetti generali, risulta ovviamente incompleta nei meccanismi di funzionamento, perfettibile nelle attribuzioni delle competenze e delle responsabilità, integrabile nella definizione degli attori coinvolti nel quadro dell’attuale legislazione, decisioni a livello nazionale che si dovranno poi coerentemente integrare con quelle a livello regionale ed aziendale. La SIHTA è altresì disponibile ad approfondire ed analizzare tali temi con tutti gli stakeholder coinvolti nel processo, in primis con i decisori politici ed istituzionali per sostenere il percorso implementativo della proposta stessa.
DECIDERE E DECIDERE CON SAGGEZZA
L’HTA è un processo multidisciplinare che analizza e sintetizza le conoscenze scientifiche sugli aspetti sanitari, sociali, economici ed etici legati all’uso di una tecnologia sanitaria per trasformale in informazioni al decisore in un modo sistematico, trasparente, obiettivo e robusto. Esso è funzionale alla formulazione di politiche sanitarie sicure ed efficaci, centrate sui pazienti e volte ad acquisire il migliore valore (EUnetHTA).
L’HTA, quindi, rappresenta lo strumento più adatto per l’SSN per migliorare i suoi processi decisionali, migliorare qualità e sostenibilità delle cure e poterne garantire l’universalismo grazie ad alcuni obiettivi assai chiari: definire ed assicurare i livelli essenziali di assistenza (LEA); gestire in modo ottimale le risorse economiche che costituiscono il fondo sanitario nazionale in uno scenario generale di crisi economica; sviluppare e diffondere nella pratica clinica tecnologie efficaci e sempre più costose, adattandosi alla transizione demografica (con l’invecchiamento della popolazione e la riduzione della natalità) ed epidemiologica (con l’aumento del carico di malattie croniche). Le grandi trasformazioni economiche e sociali in atto determinano la necessità di prendere decisioni difficili con un approccio diverso da quello attuale, a tutti i livelli del SSN (macro: pianificazione e programmazione nazionale, regionale e delle province autonome; meso: gestione delle strutture sanitarie; micro: decisioni del singolo professionista sul singolo paziente/cittadino).
PRINCIPALI CRITICITÀ NEL GOVERNO DELLE TECNOLOGIE SANITARIE IN ITALIA
Sono molte le criticità che è possibile riscontrare dall’osservazione dell’attuale sistema di governo delle tecnologie sanitarie in Italia. Tali criticità sono più spesso dovute all’architettura che l’attuale assetto istituzionale e normativo ha determinato piuttosto che alla volontà o capacità delle singole istituzioni (e dei professionisti che in esse vi operano) chiamate a svolgere un ruolo in tale contesto. Le problematiche spaziano dalla frammentazione delle competenze alla mancanza di coordinamento delle attività valutative così come dei metodi stessi (mancanza che produce una inevitabile disomogeneità dei report prodotti), dalla esiguità delle valutazioni prodotte alla loro stessa scarsa tempestività (entrambi elementi che inficiano anche la possibilità di renderle fruibili ed efficaci), dall’assenza di coinvolgimento di alcuni stakeholder alla mancata valutazione di interi comparti tecnologici, dall’esclusione delle unità di HTA ospedaliere alla disconnessione con le politiche di prezzo e le pratiche di acquisto.
In sintesi, l’HTA, sebbene presente da molti anni nelle norme, nei documenti di indirizzo e di programmazione di diverse istituzioni ai vari livelli (dal nazionale al regionale/locale), non è stato resa in grado di contribuire ed incidere come potrebbe nelle attività di governo e di innovazione delle tecnologie sanitarie, riducendo quindi le possibilità di accesso dei pazienti ai benefici garantiti dallo sviluppo tecnologico…

